Betasolusaareke mielestäni muistuttaa monella tavalla aivojen neuronaalisen kudoksen hierarkista järjestelmää ja sen tehtävänä onkin myötäillä ja heijastaa aivojen energiatarvetta ja tuottaa stabiilia aivoenergia-ainetta, verensokeria.
Sillä on siis oma endokannabinoidijärjestelmänsä minimaalisissa olosuhteissa. ( Kirjoitan tästä enemmän GLUKOOSI-blogiini)
ottaen huomoon että a) maailmassa on kiihtyvä diabetes epidemia
ja b) cannabis kiihtyvällä tahdilla konsentroidaan ja legalisoidaan
ja c) CB1-reseptori ajatellaan vain aivoasiaksi johon sitten ripustetaan kannabista ja muuta kuin joulukuuseen koristeita odotellen vain jotain tunnevastetta-
ja että d) betasolun mielipidettä kannabiksen käytöstä ei ole kysytty
-- niin katson tätä asiaa varmuuden vuoksi hieman.
Avainmolekyylinä asian kartan valkoisten läikkien hahmotatmisessa lienee ollut
rimonabantti, jota Suomessakin ehdittiin lääkkeenä käyttää jokin vuosi y liikalihavuuteen ja sitten poistettiin se lääkeaineista jo vuonna 2008.
http://dmm.biologists.org/content/9/1/51
Research Article (hiiri koe-eläimenä)
The cannabinoid CB1 receptor and mTORC1 signalling pathways interact to modulate glucose homeostasis in mice
Francisco J. Bermudez-Silva, Silvana Y. Romero-Zerbo, Magalie Haissaguerre, Inmaculada Ruz-Maldonado, Said Lhamyani, Rajaa El Bekay, Antoine Tabarin, Giovanni Marsicano, Daniela Cota
Disease Models & Mechanisms 2016 9: 51-61; doi: 10.1242/dmm.020750
Tiivistelmä ABSTRACT
Endokannabinoidisysteemi on intersellulaarinen ( solujen välinen) signaloiva mekanismi, jota esiintyy myös Langerhansin saarekkeissa ja sillä on osuutta insuliinin erityksessä ja betasolumassan lisääntymisessä
( Huom: LUONNOLLISESTI järjestelmän fysiologisin normaalein molekyylein fysiologisissa oloissa jo kymmenet tuhnnet vuodet moitteettomasti toiminut funktio. ) .
Kuitenkin tåmän järjestelmän geneettisen alavirran säätelyä on vähemmin ymmärretty ja siihen tämä tutkimus pureutuu.
Ns. mTORC -signalointi on avain asemassa oleva solun sisäinen tie, mikä on energiahomeostaasissa olennainen haimasaarekkeessakin. Tutkijat koettavat selvittää yhteydet CB1- signaloinnin ja tämän mTORC1- signaloinnin kesken.
CB1 antagonistimolekyyli on rimonabantti. Se aiheutti glukoosin stimuloiman insuliinierityksen vähenemistä.
Mutta jos mTORC1 tie estettiin (toisella aineella rapamysiini) , rimonabantin (CB1 antagonistin) estovaikutusta insuliinieritykseen ei ollut jäljellä.
Rimonabantti vähensi insuliinieritystä ja aiheutti glukoosi-intoleranssia hiiressä. (Rapamysiini pystyi kumoamaan tämänkin rimonabantti vaikutuksen) .
- The
endocannabinoid system (ECS) is an intercellular signalling mechanism
that is present in the islets of Langerhans and plays a role in the
modulation of insulin secretion and expansion of the β-cell mass. The
downstream signalling pathways mediating these effects are poorly
understood.
Mammalian target of rapamycin complex 1 (mTORC1) signalling
is a key intracellular pathway involved in energy homeostasis and is
known to importantly affect the physiology of pancreatic islets.
We
investigated the possible relationship between cannabinoid type 1 (CB1)
receptor signalling and the mTORC1 pathway in the endocrine pancreas of
mice by using pharmacological analysis as well as mice genetically
lacking the CB1 receptor or the downstream target of mTORC1, the kinase p70S6K1.
In vitro static secretion experiments on islets, western blotting, and in vivo glucose and insulin tolerance tests were performed. The CB1
receptor antagonist rimonabant decreased glucose-stimulated insulin
secretion (GSIS) at 0.1 µM while increasing phosphorylation of p70S6K1
and ribosomal protein S6 (rpS6) within the islets
Specific
pharmacological blockade of mTORC1 by 3 nM rapamycin, as well as genetic
deletion of p70S6K1, impaired the CB1-antagonist-mediated decrease in GSIS
In vivo
experiments showed that 3 mg/kg body weight rimonabant decreased
insulin levels and induced glucose intolerance in lean mice without
altering peripheral insulin sensitivity; this effect was prevented by
peripheral administration of low doses of rapamycin (0.1 mg/kg body
weight), which increased insulin sensitivity.
These findings suggest a
functional interaction between the ECS and the mTORC1 pathway within the
endocrine pancreas and at the whole-organism level, which could have
implications for the development of new therapeutic approaches for
pancreatic β-cell diseases.
--
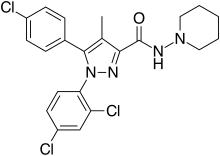
PS: Tällaisen selvityksen jälkeen saattaa ajatella että MIKÄ ON RIMONABANTIN RAKENNE?
Wikipedia kertoo.
Siinä on fenyylirenkaita joissa on klooria. Sitten siinä on karbo-ryhmä. jokin pyratsoli. Sitten N-piperidinyyli
https://books.google.se/books?id=Z36GjK1vABEC&pg=PA718&lpg=PA718&dq=N-(piperidinyl)-5-(4-chlorophenyl)-1-(2,4-dichlorophenyl)-4-methyl-1H-pyrazole-3-carboxamide&source=bl&ots=mxWT90J13F&sig=pmPVVB7B3GCxELYJuWY2yOO7Bns&hl=sv&sa=X&ved=0ahUKEwiW9YTwhtHUAhXDFJoKHX3yArIQ6AEIVDAG#v=onepage&q=N-(piperidinyl)-5-(4-chlorophenyl)-1-(2%2C4-dichlorophenyl)-4-methyl-1H-pyrazole-3-carboxamide&f=false

Inga kommentarer:
Skicka en kommentar